| Titel: | Neues Verfahren zur Schwefelsäure-Fabrication, von Professor J. Persoz in Paris. |
| Fundstelle: | Band 139, Jahrgang 1856, Nr. CI., S. 427 |
| Download: | XML |
CI.
Neues Verfahren zur
Schwefelsäure-Fabrication, von Professor J. Persoz in Paris.
Patentirt für das Königr. Hannover auf drei Jahre,
am 11. September 1855. – Aus den Mittheilungen des hannoverschen
Gewerbevereins, 1856, S. 1.
Mit einer Abbildung auf Tab. VI.
Persoz's Verfahren bei der Fabrication der
Schwefelsäure.
Wir benutzen zur Schwefelsäure-Fabrication nach neuer Methode zweierlei
Verfahrungsarten; nach der ersten erzeugen wir zuerst
schwefligsaures Gas und oxydiren dasselbe sodann; nach der zweiten zersetzen wir hingegen diese schweflige Säure mittelst feuchten
Schwefelwasserstoffs.
I. Verfahrungsart, welche auf das
oxydiren oder Säuern der schwefligen Säure gegründet ist.
Bei dieser Verfahrungsart wenden wir zwei bestimmte und den Chemikern wohl bekannte
Gegenwirkungen an:
Die erste besteht im oxydiren der schwefligen Säure (S O²) und in ihrer Verwandlung in Schwefelsäure
(SO³) durch Anwendung der Salpetersäure N²O³ + Aq, nach der Gleichung SO² + N²O⁵Aq = SO³Aq + N²O⁴
Das Verfahren aber, von dem wir Gebrauch machen, bietet diese Eigenthümlichkeit dar,
welche es von allen bis jetzt angewandten Methoden unterscheidet, daß wir die
schweflige Säure entweder in Salpetersäure führen, die ungefähr auf 100°
Cels. erhitzt ist und die zuvor mit einem vier- oder sechsmal so großen Volum
Wasser verdünnt worden ist; oder daß wir die schweflige Säure in irgend eine
Mischung von Salpetersäure und Salzsäure gelangen lassen, welche Mischung immer die
Bildung einer Quantität Königswasser (Chloruntersalpetersäure) verursacht, welche
mit der Quantität derjenigen Säure im Verhältniß steht, die den schwächern Theil der
Mischung bildet.
Die zweite besteht im Oxydiren des
Untersalpetersäure-Dampfes (N²O⁴) oder des
Chloruntersalpetersäure-Dampfes (N²O²Cl²), und in
seiner Verwandlung in Salpetersäure (N²O⁵)
vermittelst des aus der Luft oder von irgend einer andern Quelle herrührenden
Sauerstoffs.
Bekanntlich verbinden sich nach einer Reihe aufeinanderfolgender, bei Gegenwart des
Wassers oder des Wasserdampfes stattfindenden Wirkungen, vier Theile
Untersalpetersäure-Dampf (N²O⁴) und ein Theil Sauerstoff zu Salpetersäure
(N²O⁵).
Wir benutzen diese Wirkung, um den Untersalpetersäure-Dampf zu oxydiren und
auf diese Weise die Salpetersäure wieder zu bilden, im Augenblicke selbst, wo ihre
Zersetzung stattgefunden hat, und zwar nach Belieben entweder in demselben Gefäße,
wo die schweflige Säure oxydirt wird, damit die größtmögliche Quantität
Schwefelsäure darin angesammelt werde, oder in einem Nebengefäße, mit welchem das
erste in Verbindung steht, wenn dieses oxydiren nicht mehr auf eine vortheilhafte
Weise in dem ersten Gefäße stattfinden kann. Auf diese Art ist die Erzeugung der
Schwefelsäure ununterbrochen, indem die Salpetersäure bald auf einem, bald auf dem
anderen Punkte wirkt.
Diese neue Methode, die schweflige Säure zu oxydiren, gewährt folgende Vortheile:
a. Wir schaffen die Bleikammern ganz ab.
b. Wir benutzen zur Fabrication der Schwefelsäure nicht
bloß die schweflige Säure, welche durch die Verbrennung des Schwefels oder gewisser
Kiese erzeugt wird, wie es beim gewöhnlichen Verfahren mit Bleikammern der Fall ist,
sondern auch die schweflige Säure von irgend einer chemischen Reaction herrührend,
welche sie entweder rein oder in verschiedenen Verhältnissen mit Stickstoff,
Kohlensäure, Kohlenoxyd, Wasserstoff oder Kohlenwasserstoff vermischt liefert.
c. Wir benutzen bis ins Unendliche wieder dieselbe
Salpetersäure, welche wir zur Bereitung der Schwefelsäure angewandt haben, und die
einzigen Verluste sind diejenigen, welche bei jeder Bewegung der Materie
unvermeidlich sind.
d. Unsere Verfahrungsarten lassen sich mit Vortheil beim
Ausziehen der Metalle anwenden.
e. Wir verwandeln das salpetersaure Kali und das
salpetersaure Natron, und auch die Chloride dieser Alkalien in schwefelsaures Kali
und schwefelsaures Natron, nachdem jene Salze zuvor in Wasser aufgelöst worden sind,
welches (für die salpetersauren Salze) ein gewisses Verhältniß von Salzsäure oder
(für die Chloride) eine gewisse Quantität Salpetersäure enthält, damit in beiden
Fällen die Chloruntersalpetersäure erzeugt werde, welche die nöthige Quantität schweflige Säure in
Schwefelsäure verwandeln muß, um die ganze Grundlage des salpetersauren Salzes oder
des Chlorids in ein schwefelsaures Salz zu verwandeln. Sobald dieses Resultat
erlangt ist, genügt es, die Flüssigkeit in Destillirapparaten zu concentriren, um
die überflüssige Salzsäure oder Salpetersäure auszutreiben.
Die Reaction, die wir eben für solche Salze beschrieben haben, welche die
Alkalimetalle bilden, kann eben so gut zur Zersetzung der anderen salpetersauren
Salze oder Chlorverbindungen angewandt werden.
f. Da wir die schweflige Säure ebensowohl im reinen
Zustande wie mit anderen Gasen vermischt gebrauchen können, so können wir zu unserem
Zweck jenes Gas auf folgende Arten erhalten:
1) Durch das Rösten aller Sorten geschwefelter Erze, indem man,
bevor man die schweflige Säure in die Salpetersäure treten läßt, die verdichtbaren
Dämpfe, wie z.B. arsenige Säure (As²O³), in dazu geeigneten Gefäßen
niederschlägt.
2) Durch die Reaction der Schwefelsäure oder des sauren
schwefelsauren Kalis oder Natrons auf gewisse Metalle, oder auf natürliche Sulfide
oder Arsensulfide.
3) Durch die Reaction des schwefelsauren Eisenoxyduls,
Eisenoxyds, Zinks und Kupfers auf die correspondirenden Sulfide derselben Metalle
bei einer passenden Temperatur und in irdenen oder in gußeisernen
Destillirgefäßen.
4) Durch die Zersetzung der Eisenoxydul-,
Eisenoxyd-, Zink- und Kupfer-Sulfate, entweder mittelst Kohle
oder mittelst Wasserstoff oder Kohlenoxyd, oder auch durch Kohlenwasserstoff.
Diese Zersetzung muß für jedes solche schwefelsaure Salz bei einem
genügend hohen Wärmegrad stattfinden, damit die Schwefelsäure zersetzt und als
schwefligsaures Gas ausgetrieben werde, und endlich nur ein Metall oder ein Metalloxyd zurückbleibt, aus
welchem Oxyd man das Metall immer wieder herstellen kann. Wenn man z.B.
schwefelsaures Kupferoxyd in einem Strom von reinem oder mehr oder weniger
kohlehaltigem Wasserstoff auf eine Temperatur von 220 bis 250° Cels. erhitzt,
so verschwindet die ganze Schwefelsäure dieses Salzes als schwefligsaures Gas mit
Kohlensäure vermischt, und es bleibt reines Kupfer zurück (mit schwefelsaurem
Eisenoxydul oder Zink vermischt, wenn das schwefelsaure Kupfer solche Salze oder
schwefelsaures Eisenoxyd enthielt). In diesen verschiedenen Fällen werden immer die
Salze aus dem Rückstand ausgelaugt.
5) Durch die Reaction des salzsauren Gases (H²Cl²) auf
schwefelsauren Kalk.
6) Durch die Verbrennung des unreinen Schwefels, welcher als
Rückstand bei der Behandlung gewisser natürlicher Sulfide mit Salpetersäure erhalten
wird.
II. Verfahrungsart, welche auf der
Zersetzung der schwefligen Säure durch die Schwefelwasserstoffsäure gegründet
ist.
Es ist bekannt, daß das schwefligsaure Gas (SO²)
und das Hydrothion-Gas (H²S), bei der Berührung mit Wasser oder Wasserdampf,
einander zersetzen, indem sie folgende Producte erzeugen:
1) Einen Schwefelniederschlag.
2) Eine gewisse Quantität Schwefelsäure.
3) Einen starken Antheil unterschwefliger Säure, welche durch
die Hitze zersetzt wird, wodurch Schwefel, schweflige Säure und Schwefelsäure
erhalten werden; wird aber die unterschweflige Säure mit salpetriger Säure oder
Untersalpetersäure behandelt, so wird sie nur in Schwefel und Schwefelsäure
verwandelt.
Diese Reactionen benutzen wir:
1) wenn das Rösten der geschwefelten Erze Gase erzeugt, welche
zu wenig schweflige Säure enthalten, um diese Säure mit Vortheil nach der oben
beschriebenen Methode durch die Salpetersäure oxydiren zu können;
2) wenn man, zu einem industriellen Zweck, natürliche oder
künstliche Sulfide durch eine Säure zu zersetzen wünscht, um entweder Schwefel oder
Metall auszuziehen.
Was die Reaction der Gase betrifft, so findet sie für beide Verfahrungsarten in den
Apparaten statt, die wir jetzt beschreiben werden.
Princip der Einrichtung der Apparate.
Sehr verschiedenförmige Apparate können zur Fabrication der Schwefelsäure durch
unsere Verfahrungsarten angewandt werden; wir wollen hier die drei wesentlichen
Theile erläutern, aus welchen unsere Apparate bestehen, in der Voraussetzung,
daß wir die erste Verfahrungsart anwenden.
Der erste Theil bezieht sich auf die Erzeugung der
schwefligen Säure. Dazu benutzen wir Apparate wie sie zur Destillation der
organischen Substanzen, der Steinkohle etc. dienen; diese Apparate verwenden wir
zum Rösten und
zum Oxydiren der Erze, mit oder ohne Blasemaschine, um die nöthige Luft
einzublasen.
Der zweite Theil hat zum Hauptzweck, die möglichst
unmittelbare Berührung der schwefligen Säure und der Salpetersäure zu erlangen.
Alle Apparate, die dazu gebraucht werden um ein Gas und eine Flüssigkeit in
Berührung zu setzen, können in diesem Falle angewandt werden.
Als Material der Gefäße benutzen wir Lava, Granit,
Glas, solche Erden, welche durch die Säuren nicht angegriffen werden,
natürlichen oder künstlichen Sandstein, gehärteten Kautschuk,
Gutta-percha und überhaupt alle Substanzen, welche durch die
zusammengemischten Säuren: Schwefelsäure, Salpetersäure und Untersalpetersäure
nicht angegriffen werden.
Der dritte Theil des Apparats hat einen doppelten
Zweck:
1) Die Berührungspunkte des Untersalpetersäure-Dampfes
mit der Luft, dem Wasser oder dem Wasserdampfe zu vermehren, damit die
Salpetersäure beinahe im selben Augenblicke, wo sie zersetzt wird, wieder
hergestellt werde.
2) Den Stickstoff, die überflüssige Luft und die kohlehaltigen
Gase, welche mit der schwefligen Säure vermischt seyn können, von der
Salpetersäure zu befreien, welche sie enthalten.
Bei unserer Verfahrungsart wird dieses doppelte Resultat vermittelst eines
Bewegungsapparates erlangt, der sich in dem Gefäße befindet, in welchem die
schweflige Säure oxydirt wird, und mit Hülfe eines Schornsteins, dem man die
nöthige Höhe geben kann, damit die Gase von selbst darin steigen; indem sie
durch poröse Substanzen, die fortwährend durch einen herunterfließenden
Wasserstrom genäßt sind, zertheilt werden, sind diese Gase, wenn sie oben
ankommen, genug von der Salpetersäure befreit.
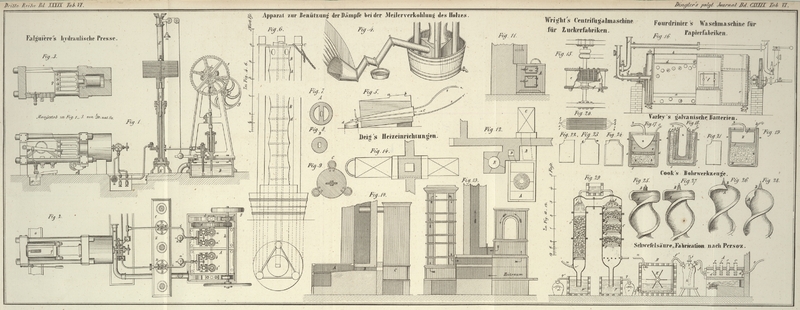
Beschreibung des Apparats.
Dieser, in Fig.
29 abgebildete Apparat, besteht aus drei Haupttheilen A, B, C.
Der Theil A, dessen Form und Einrichtung sehr
verschieden seyn kann, nach der Natur oder dem Zustande der Materialien, die man
benutzt, ist derjenige in welchem die schweflige Säure erzeugt wird, die zur
Fabrication der Schwefelsäure nöthig ist.
Der Theil B ist dazu bestimmt, die schweflige Säure
und die mit der sechsfachen Quantität Wasser verdünnte Salpetersäure bei der
geeigneten Temperatur in unmittelbare Berührung zu bringen.
Der Theil C ist eine Art Kamin, in welchem alle
gasförmigen Körper, die der in B stattfindenden
Reaction entgehen, durch Oeffnungen
o ankommen, um dort ihre gegenseitigen Wirkungen zu
vollenden und zuletzt Salpetersäure herzustellen, welche mit einem kleinen
Antheil von Schwefelsäure vermischt ist und in einem unteren Behälter p aufgenommen wird.
Was den Stickstoff betrifft, sowie die im Uebermaaß angewandte Luft, die
Kohlensäure, das Kohlenoxyd und die anderen Gase, welche die schweflige Säure
bei ihrer Bildung begleiten könnten, so steigen sie in den Schornstein, in
welchem sie durch die porösen und feuchten Körper, die sich darin befinden, von
den letzten Säuretheilchen, die sie noch enthalten könnten, befreit werden; dann
fließen sie aus in die Atmosphäre, oder wenn man es für nöthig hält, kann man
sie durch einen zweiten Kamin, welcher ebenfalls mit porösen Substanzen, z.B.
Bimsstein, gefüllt wäre, vermittelst eines saugenden Apparats wieder
herunterziehen lassen.
Für die Verbrennung des Schwefels, welche nicht mehr in der freien Luft, wie bei
der gewöhnlichen Verfahrungsart stattfinden kann, haben wir die Einrichtung
angenommen, die wir für den ersten Theil A des
Apparates in Fig. 29 dargestellt haben; wir wenden nämlich gußeiserne Cylinder
oder besser noch irdene Retorten d an, denjenigen
ähnlich, die man zur Destillation des Leuchtgases benutzt. Diese Gefäße dienen
dann als Verbrennungskammern und werden durch einen Herd g geheizt.
Durch das eine Ende der Retorten wird Luft vermittelst einer Blasemaschine oder
eines Ventilators durch ein Rohr e hineingetrieben,
während die schweflige Säure am andern Ende herauskommt, um durch ein Rohr f durch die Salpetersäure geführt zu werden, in
welcher sie oxydirt werden muß.
Da die Verbrennung des Schwefels somit in einem Gefäße stattfindet, in welchem
nur eine beschränkte sich bewegende Luftmasse enthalten ist, so ist es wichtig,
eine Verflüchtigung des Schwefels zu vermeiden.
Nach vielen Versuchen haben wir folgendes Verbrennungssystem angenommen: wir
lassen in das Innere der Retorte durch ihren oberen Theil eine Reihe von Röhren
hineindringen, welche aus porösem Thon gemacht und an ihren unteren Enden im
Innern der Retorte verschlossen sind, während ihr oberstes Ende in der freien
Luft offen ist und um 1 bis 1 1/2 Fuß vorspringt.
Nachdem diese Röhren oder Cylinder in die Oeffnungen der Retorte gut eingesetzt
worden sind, füllt man sie mit Schwefel.
Wenn man dann die Retorte an ihrem untern Theil heizt, so schmilzt der Schwefel
bald, er schweißt durch die porösen Röhren und endlich entzündet er sich.
So ist jeder kleine Cylinder nur im Innern der Retorte mit einer Flamme bedeckt,
welche regelmäßig durch die hereingeblasene Luft und durch das Schweißen des
Schwefels unterhalten wird, welches auf dieselbe Weise geschieht, wie das
Durchschwitzen des Wassers in den spanischen kühlenden Krügen.
Das Rohr f, anstatt direct zum Mischungsapparat zu
gelangen, welcher der zweite Theil der ganzen Einrichtung ist, steht mit einer
von den drei Tubulaturen i des Zwischengefäßes h in Verbindung, welches aus Glas oder Thon gemacht
ist.
Die mittlere Tubulatur empfängt ein Luftrohr j,
welches mit einem Hahne versehen ist, um in dieses Gefäß eine solche Quantität
Luft hereinzuführen, daß das Volum des darin enthaltenen Sauerstoffs halb so
groß ist, als das der schwefligen Säure, welche vom Apparate A kommt.
Die dritte Tubulatur ist mit dem Rohre f¹
verbunden, welches dann alle Säure und die Luft in den Mischungsapparat B führt und sie in der ganzen flüssigen Masse
vertheilt, indem der untere Theil dieses Rohres, welcher in die Flüssigkeit
taucht, mit einer Reihe von kleinen Löchern versehen ist.
Die Flüssigkeit besteht, wie bemerkt, aus Salpetersäure und Wasser, und die
Mischung wird fortwährend durch die Flügel des Rades K bewegt, welches sich im Innern des Apparats mit einer passenden
Schnelligkeit dreht.
Der Behälter B, welcher das Ganze enthält, ist aus
zwei Stücken gemacht, damit er leicht auseinander genommen und wieder
zusammengestellt werden kann. Er kann im Nothfalle durch einen besonderen Herd,
oder durch Dampf, erhitzte Luft etc. auf die erforderliche Temperatur gebracht
werden.
An seinem unteren Theile ist ein Hahn l angebracht,
welcher ihn auszuleeren gestattet, wenn es nöthig ist, und an seinem obern Theil
ist eine Tubulatur m, die das Rohr n empfängt, welches sich (wie es in der Zeichnung
dargestellt ist) bis zum unteren Theile des Schornsteins C verlängert, den wir den Wiederhersteller
der Salpetersäure nennen können.
Aus der Zeichnung ersieht man, daß dieser Apparat mit mehreren gleichen
Oeffnungen o versehen ist, um mehrere Röhren zu
empfangen, und daß er sich unten verlängert um in das Gefäß p zu dringen, welches mit einem Ueberlaufrohre q versehen ist, um die überlaufende Salpetersäure in
den Krug r zu ergießen.
Das Innere des Wiederherstellers C enthält
durchlöcherte Querbleche s, wodurch Abtheilungen
gebildet werden, die die porösen Körper enthalten, von denen wir schon
gesprochen haben, und durch welche die Säuren steigen, welche vom
Mischungsapparate kommen.
An seinem obersten Ende empfängt der Kamin durch ein Rohr t Wasser, welches sich auf der ganzen Oberfläche vertheilt, um die
Salpetersäure in das unterste Gefäß mit sich fortzureißen.
Ein zweiter Kamin C¹, dem ersten ähnlich und
mit ihm in Verbindung stehend, kann die beschriebene Arbeit vervollständigen,
indem die Gase durch diesen zweiten Kamin C¹
von oben nach unten ziehen, bevor sie sich zum saugenden Apparate u begeben.
Ein Gefäß p¹, ebenfalls mit einem Ueberlaufe
q¹ versehen, sammelt die Salpetersäure
auf, und mit ihr die geringe Menge Schwefelsäure, welche in diesen letzten
Apparat mit fortgerissen werden konnte.
Tafeln