| Titel: | Neue Verfahrungsweisen zur Prüfung der Säuren, insbesondere des Essigs, ferner des Braunsteins; von Dr. R. Fresenius und Dr. H. Will. |
| Fundstelle: | Band 90, Jahrgang 1843, Nr. LIII., S. 210 |
| Download: | XML |
LIII.
Neue Verfahrungsweisen zur Pruͤfung der
Saͤuren, insbesondere des Essigs, ferner des Braunsteins; von Dr. R. Fresenius und Dr.
H. Will.Auszug aus dem Werke der Verfasser: „Neue Verfahrungsweisen zur Pruͤfung der
Potasche und Soda, der Aschen, der Saͤuren etc.
Heidelberg bei C. F. Winter
1843.“
(Beschluß der im vorhergehenden Heft S. 144
enthaltenen Abhandlung.)
Mit Abbildungen auf Tab.
III.
Fresenius u. Will, neue Verfahrungsweisen zur Bestimmung des
Werthes der Säuren und des Braunsteins.
I. Prüfung
der Säuren auf ihren Handelswerth.
Fast alle Säuren, welche als Handelsartikel Bedeutung haben, sind Gemische von reiner
Säure mit Wasser in wandelbaren Verhältnissen und ihr Werth ist proportional ihrem
Gehalt an wasserfreier Säure. Um leztern zu ermitteln, sind verschiedene rein
chemische Prüfungsmethoden in Vorschlag gekommen, welche sämmtlich darauf beruhen,
daß die Säure mit einem Alkali gesättigt und die verbrauchte Menge des leztern
bestimmt wird. In der Art der Ausführung weichen diese Methoden nach verschiedenen
Richtungen von einander ab.
Entweder nämlich bereitet man sich eine nach Art der Gay-Lussac'schen Probesäure titrirte
Auflösung eines Alkalis (Kalk, Ammoniak, kohlensaures Natron) und bestimmt die
verbrauchte Menge wie bei jener durch Maaß, oder man wägt eine bestimmte Menge eines
in Wasser unlöslichen Sättigungsmittels (gewöhnlich reinen Kalkspath) ab, bringt die
Säure damit in Berührung bis sie neutralisirt ist, und bestimmt alsdann aus der
Gewichtsabnahme des Kalkspaths die Menge des verbrauchten kohlensauren Kalks, aus
welcher sich der Gehalt der Säure alsdann durch einfache Rechnung finden läßt.
— Die erstere Verfahrungsweise hat mit den alkalimetrischen Methoden Descroizilles', Gay-Lussac's u. s. w. die meisten Unvollkommenheiten gemein;
ihre Resultate verändern sich mit der Temperatur, bei welcher die Probe vorgenommen
wird, indem sich sowohl das Volum der Säuren als das der Probeflüssigkeit mit
derselben vergrößert oder verringert; sie werden schwankend, weil es schwierig ist,
den Sättigungspunkt stets mit gleicher Sicherheit zu treffen; sie werden unrichtig,
wenn die alkalische Probeflüssigkeit nicht mit größter Sorfalt bereitet oder die
Meßinstrumente nicht völlig genau sind. — Die andere Prüfungsweise hat den
Uebelstand, daß sich schwache Säuren auch bei langer Digestion mit Kalkspath, sogar
beim Erwärmen nicht
ganz vollständig sättigen, so wie daß der Kalkspath nicht allein von der
abzustumpfenden Säure, sondern auch von der frei werdenden Kohlensäure aufgelöst
wird — zwei Fehler, die genaue Resultate unmöglich machen und die noch weit
mehr ins Auge fallen würden, wenn nicht einer den andern einigermaßen
compensirte.
Princip der neuen Methode. — Die Methode, welche
wir zur Gehaltprüfung der Säuren in Vorschlag bringen, hat eine von denen der
bisherigen Methoden völlig verschiedene Grundlage. Sie beruht auf der Bestimmung der
Kohlensäure, welche durch eine gewogene Menge der zu prüfenden Säure ausgetrieben
wird; sie läßt sich zur Bestimmung aller Säuren anwenden, welche kohlensaures Natron
vollständig zerlegen, gleichgültig ob dieselben Salze oder organische Materien
aufgelöst enthalten oder nicht; ihre Ausführung ist wo möglich noch einfacher als
die unseres alkalimetrischen Verfahrens; ihre Genauigkeit läßt, wie wir uns
überzeugt haben, nichts zu wünschen übrig. — Einen
Uebelstand hat sie jedoch mit den übrigen acidimetrischen Methoden gemein, nämlich
den, daß sie eben so wie diese freie Schwefelsäure, wenn sie im Essig enthalten
istUeber die Pruͤfung des Essigs auf Verfaͤlschungen wurde im
vorhergehenden Heft des polytechn. Journals S. 119 eine Abhandlung
mitgetheilt. A. d. R. als Essigsäure, — Salzsäure, welche
in der Salpetersäure enthalten ist, als Salpetersäure u. s. w. finden läßt. Daß
also, wenn man sich nicht der Gefahr aussezen will, nach dieser Seite hin Fehler zu
machen, auch bei Anwendung unserer Methode die gewöhnlichen qualitativen Prüfungen
auf die Reinheit der Säuren vorausgehen müssen, versteht sich von selbst.
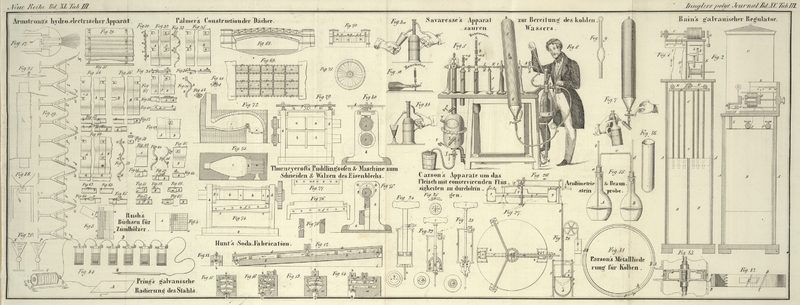
Zur Ausführung der Kohlensäurebestimmung bedient man sich des nämlichen Apparates,
welchen wir zur Alkalimetrie gebrauchen. Man wählt für A
ein Kölbchen, welches wenigstens 6 Loth Wasser faßt und eine möglichst weite aber
dabei vollkommen runde Mündung hat. Außer diesem Apparate Fig. 85
Tab. III hat man noch ein kleines Glasröhrchen Fig. 86 und
doppelt kohlensaures Natron nöthig.
Das Glasröhrchen verfertigt man sich entweder aus einem größeren Glasrohre, am
einfachsten aber durch Abfeilen des hinteren Endes eines engen Probecylinders.
Seiner Weite nach muß es leicht in den Hals des Kölbchens A eingeschoben, seiner Länge nach horizontal auf den Boden desselben
gelegt werden können, seinem Inhalte nach fasse es 4–5 Gramme doppelt
kohlensauren Natrons. — Was das leztere anbetrifft, so ist es nicht
nothwendig, daß es absolut rein, d. h. von schwefelsaurem Natron und Chlornatrium
völlig frei sey, eben so ist es gleichgültig, ob es troken oder feucht ist.
Eine Bedingung aber ist wesentlich, nämlich die, daß es
vollkommen doppelt kohlensauer sey, daß es also kein einfach oder anderthalbfach
kohlensaures Natron enthalte; von ihrer Erfüllung hängt die Richtigkeit des
Resultats, das Gelingen der Prüfungen ab. — Ehe man daher ein doppelt
kohlensaures Natron zu einer Versuchsreihe bestimmt, muß es zuvor einer sorgfältigen
Prüfung unterworfen werden.
Zu pharmaceutischem Gebrauche prüft man das doppelt kohlensaure Natron, indem man
seiner Lösung eine Solution von Queksilbersublimat zusezt; entsteht beim
Zusammenkommen beider im Anfange nur eine weiße Trübung, so erklärt man es für rein.
Diese Prüfungsweise ist keineswegs sehr genau, wovon man sich leicht überzeugt, wenn
man zu doppelt kohlensaurem Natron etwas einfach kohlensaures sezt und dann mit
Sublimat prüft. Ist die zugesezte Menge des einfach kohlensauren Kalis nicht
ziemlich erheblich gewesen, so erhält man von Anfang immer nur eine weiße Trübung.
Auf diese Reaction kann man sich demnach nicht verlassen, sondern man muß eine
andere Prüfungsweise wählen, wenn man seiner Sache gewiß seyn will. Da diese aber
ein wenig mehr Zeit in Anspruch nimmt, so daß öftere Wiederholung derselben
möglichst vermieden werden muß, so ist es sehr zu empfehlen, das käufliche doppelt
kohlensaure NatronStatt des Natronsalzes kann eben so gut doppelt kohlensaures Kali genommen
werden; das erstere verdient jedoch nicht nur seiner groͤßeren
Billigkeit wegen (in Preiscouranten ist das Natronsalz zu 24 bis 30 Kreuzer
notirt, waͤhrend der Preis des Kalisalzes fast das doppelte
betraͤgt), sondern auch deßwegen vorgezogen zu werden, weil es im
Vergleich mit dem Kalisalz eine groͤßere Quantitaͤt
Kohlensaͤure entwikelt. zuvor einer Reinigung zu
unterwerfen. Man verwandelt zu dem Behufe ½ Pfd. bis 1 Pfd. desselben in ein
gleichförmiges Pulver, prüft es vor Allem nach der obigen Methode mit
Sublimatlösung, übergießt es, falls man es probehaltig gefunden hat, in einem Glase
mit der gleichen Menge kalten Regenwassers, läßt unter wiederholtem Umrühren 24
Stunden stehen, bringt das Salz sodann auf einen Trichter, in den man ein wenig
Baumwolle gestekt hat, läßt die Lauge abtropfen und wascht noch einigemal mit
kleinen Quantitäten kalten Regenwassers nach. — So behandeltes doppelt
kohlensaures Natron ist in der Regel rein und zu den acidimetrischen Versuchen
geeignet.
Man troknet es zwischen Fließpapier an der Luft ohne Anwendung von Wärme und hebt es
zum Gebrauche in einem verschlossenen Glase auf. — Will man sich nunmehr, was
immer das sicherste ist, von seiner Reinheit durch einen directen Versuch
überzeugen, so wägt man, ohne es vorher auf irgend einen Zustand bestimmter
Trokenheit gebracht zu
haben, zwei gleiche Theile (etwa 4 Gramme jedesmal) ab, bestimmt im einen Theil nach
der bei der Alkalimetrie angegebenen Methode die Kohlensäure, den andern bringt man
in ein Schälchen oder in einen kleinen Tiegel von Platin oder Porzellan, erhizt über
einer Spirituslampe allmählich bis zum Glühen, wägt, nimmt das Salz heraus, bestimmt
das Gewicht des leeren Schälchens und findet so das Gewicht des Rükstandes. Verhält
sich die Menge desselben zu der der gefundenen Kohlensäure wie 666:550, oder weicht
das gefundene Verhältniß wenig von dem angegebenen ab, so ist das Salz zum
vorliegenden Zwek geeignet, im andern Falle muß es verworfen werden. — Prüft
man auf gleiche Weise doppelt kohlensaures Kali, so ist das zu findende relative
Verhältniß des Rükstands zur entwichenen Kohlensäure wie 865:550.
Ausführung. — Das Verfahren selbst besteht in
Folgendem. Man wägt nach der S. 130 (im vorhergehenden Heft des polytechn. Journals)
angegebenen Methode im Kölbchen A (Fig. 85
Tab. III) eine bestimmte Menge SäureUm eine Fluͤssigkeit auf leichte Weise vollkommen genau zu
waͤgen, gießt man, indem man die Schale, auf welcher das
Gefaͤß steht, mit dem Finger niederdruͤkt, so lange zulezt
tropfenweise zu, bis die Schale eben sinkt, und entfernt alsdann den
Ueberschuß, indem man ein duͤnnes Glasstaͤbchen eintaucht, den
daran haͤngen gebliebenen Tropfen entfernt und dieß wiederholt, bis
das Gleichgewicht hergestellt ist. ab (die für die verschiedenen
Säuren passendsten Quantitäten sind unten S. 217 angegeben), sezt, im Falle man mit
concentrirten Säuren zu thun hat, je nach dem Grade der Concentration die
vier- bis achtfache Menge oder im Allgemeinen so viel Wasser hinzu, daß die
gesammte Flüssigkeit ¼ bis ⅓ des Inhalts von A einnimmt, füllt alsdann das Glasröhrchen bis beinahe zum Rand in der Art
mit doppelt kohlensaurem Natron, daß man dasselbe mit einem kleinen Holze fest
eindrükt, bindet um das Röhrchen nahe an seinem offenen Ende einen Seidenfaden, läßt
es an diesem in das die zu untersuchende verdünnte Säure enthaltende Kölbchen A hinab, so daß es darin aufrecht hängend schwebt und
verschließt alsdann das Kölbchen mit seinem Korke, so daß der Seidenfaden
eingeklemmt wird. Der Apparat ist im Uebrigen gerade wie es früher beschrieben
wurde, mit Schwefelsäure gefüllt und zugerüstet. — Derselbe wird jezt (ist
durch das Vermischen einer concentrirten Säure mit Wasser die Flüssigkeit warm
geworden, so muß man sie zuvor vollständig erkalten lassen) auf der Waage ins
Gleichgewicht gebracht. Man lüpft alsdann den Stopfen des Kölbchens A, läßt das Röhrchen sammt dem Seidenfaden in die Säure
fallen und dreht nunmehr den Kork schnell und fest ein.
Die Entwikelung der Kohlensäure beginnt alsobald, sie dauert, ohne daß man irgend
etwas an dem Apparat zu machen braucht, ununterbrochen und gleichmäßig fort, bis die
Säure vollständig neutralisirt ist. Durch von Zeit zu Zeit wiederholtes Umschütteln
läßt sie sich beschleunigen. Ist sie völlig beendigt, kommen also beim Umschütteln
keine Gasblasen mehr, was selbst bei sehr schwachen Essigen nie länger als eine
Stunde dauert, so stellt man das Kölbchen A bis an den
Hals in ein Glas oder einen kleinen Topf mit Wasser, welches so heiß ist, daß man
den Finger eben noch, aber kaum, hinein halten kann, läßt es unter öfterem
Umschütteln darin, bis die neuerdings eingetretene Gasentwikelung vollständig
aufgehört hat, lüpft alsdann das Wachsstöpfchen auf der Röhre a (sonst würde beim Herausnehmen die Schwefelsäure zurüksteigen), nimmt
den Apparat aus dem warmen Wasser, troknet ihn ab und saugt unmittelbar darauf so
lange ganz langsam Luft hindurch, bis man bei fortgeseztem Durchsaugen keine
Kohlensäure mehr schmekt.
Der Apparat wird nach dem Erkalten und nachdem er ganz sorgfältig abgetroknet worden,
wiederum auf die Waage gestellt, die Tara auf die andere Schale gebracht und die
entwichene Kohlensäure durch Gewichte ersezt. Aus dem Gewicht der Kohlensäure findet
man die Menge wasserfreier Säure, welche in der verwendeten Quantität wasserhaltiger
enthalten war, durch folgenden Ansaz:
Zwei Mischungsgewichte Kohlensäure verhalten sich zu einem Mischungsgewichte der in
Frage stehenden wasserfreien Säure wie die gefundene Menge Kohlensäure zu der
gesuchten Menge wasserfreier Säure. Hätten wir z. B. verdünnte Schwefelsäure geprüft
und 1,5 Gramme Kohlensäure bekommen, so erhielten wir den Ansaz:
550 (2×275) : 501
=
1,5 : x
x
=
1,36.
In der abgewogenen Menge Schwefelsäure wären demnach 1,36 Gramme wasserfreier Säure
enthalten gewesen. Sezen wir den Fall, diese abgewogene Quantität habe 15 Gramme
betragen, so hätte die geprüfte Schwefelsäure einen Procentgehalt von 9,06, denn
15 : 1,36
=
100 : x
x
=
9,06.
Um übrigens jede Rechnung überflüssig zu machen, werden wir S. 217 die Mengen
anführen, welche von den verschiedenen Säuren genommen werden müssen, damit aus dem
Gewicht der Kohlensäure der Procentgehalt der geprüften Säure sich unmittelbar
ergibt.
Dem doppelt kohlensauren Natron kann einfach kohlensaures nicht substituirt werden,
weil sich bei Anwesenheit des lezteren bei der Operation selbst doppelt kohlensaures
Salz bilden würde, in Folge welches Umstandes man viel zu wenig Kohlensäure fände,
indem die Lösung des doppeltkohlensauren Natrons sogar bei längerem Kochen der
Flüssigkeit ihr zweites Mischungsgewicht Kohlensäure nicht vollständig abgibt.
Abgesehen davon gewährt das doppelt kohlensaure Natron auch noch den wesentlichen
Vortheil, daß man für ein Aequivalent Säure immer zwei Aequivalente Kohlensäure
erhält, daß also der Gewichtsunterschied des Apparates vor und nach der Operation
gerade noch einmal so groß wird, als wenn man einfach kohlensaures Natron angewendet
hätte — ein Umstand, der zur Genauigkeit der Resultate wesentlich beiträgt,
indem alle aus dem Wägen hervorgehenden Fehler halbirt werden.
Die Annehmlichkeit bei dieser Operation ist, daß sie sich, einmal eingeleitet, von
selbst beendigt, ohne daß man nöthig hat ihr weitere Aufmerksamkeit zu schenken. Ein
Zurüksteigen der Schwefelsäure ist unmöglich, weil sich der Inhalt des Kölbchens A bei Anwendung von verdünnten Säuren nicht erwärmt,
sondern im Gegentheil kälter wird.
Das Erwärmen nach beendigter Operation ist unerläßlich, will man nicht jedesmal 25
bis 30 Milligramme Kohlensäure zu wenig erhalten.
Davon, daß aus der Flüssigkeit in A durch das Erwärmen
und die hindurchgesaugte Luft so gut wie alle Kohlensäure ausgetrieben wird,
überzeugt man sich leicht, wenn man einen Apparat nach einmaligem Erwärmen und
Durchsaugen genau tarirt, alsdann wiederum erwärmt und nochmals, und zwar anhaltend,
durchsaugt. Man wird finden, daß sein Gewicht nicht mehr, oder höchstens um ein
unerhebliches (nach unseren Erfahrungen in der Gränze von 1 bis 10 Milligrammen)
abnimmt. Durch diese Thatsache wird gleichzeitig der Beweis geliefert, daß aus einer
Lösung von doppelt kohlensaurem Alkali, als welche die nach der Operation im
Kölbchen bleibende Flüssigkeit zu betrachten ist, durch die genannten Operationen
keine in Betracht kommende Menge von Kohlensäure hinweggeführt wird. — Das
Durchsaugen muß jedoch ganz langsam geschehen, denn bei stürmischem Durchstreichen
der Luft würden Tröpfchen der doppelt kohlensaures Alkali enthaltenden Flüssigkeit
in die Schwefelsäure hinübergerissen, woselbst sie ihre Kohlensäure verlören und
somit natürlicherweise einen größeren Gewichtsverlust des Apparates veranlaßten.
Eine Sache, auf die wir kaum glauben aufmerksam machen zu müssen, ist die, daß man
immer eine zur Sättigung der Säure mehr als hinlängliche Menge doppelt kohlensauren
Alkalis anwenden muß, daß man also erhaltene Resultate nicht eher als richtig
betrachten darf, bis man sich nach beendigter Operation durch ein in das Kölbchen A geworfenes Streifchen Lakmuspapier überzeugt hat, daß die Flüssigkeit in
demselben nicht mehr sauer reagirt. Diese Prüfung wird überflüssig, wenn sich in dem
Glasröhrchen noch ungelöstes doppelt kohlensaures Natron befindet, wie dieß in der
Regel der Fall ist. Wenn gleich es nun schwierig ist, allgemein gültige Regeln zu
geben, wie viel Säure man abwägen solle, damit das doppelt kohlensaure Natron im
Röhrchen mehr als hinreichend sey, so ist doch nichts leichter, als dieses
Verhältniß nach einer ganz oberflächlichen vorläufigen Beurtheilung des
Concentrationsgrades der Säure zu treffen, indem ja ein Ueberschuß von doppelt
kohlensaurem Natron in keiner Weise nachtheilig ist. Sollte man finden, daß das nach
Vollendung des Versuchs in A geworfene Lakmuspapier noch
geröthet wird, so müßte man ein zweites Röhrchen mit doppelt kohlensaurem Natron
füllen, dasselbe für sich auf derselben Waagschale tariren, auf der man den Apparat
zuvor gewogen hat, die Tara des Röhrchens mit der ursprünglichen des Apparates
vereinigen, das Röhrchen aber geradezu in das Kölbchen A
fallen lassen. Alles Uebrige bliebe sich gleich.
Bei der Untersuchung anzuwendende Quantitäten der einzelnen
Säuren. — Um aus der gefundenen Menge Kohlensäure ohne eine
Gleichung den Gehalt der am häufigsten vorkommenden Säuren an wasserfreier Säure
finden zu können, wollen wir nun die Mengen angeben, welche von den einzelnen zu
nehmen sind, damit die Anzahl der Centigramme, welche für die entwichene Kohlensäure
auf die Waage gelegt werden müssen, die Procente wasserfreier Säure in der geprüften
wasserhaltigen unmittelbar angibt.
Anstatt der angegebenen Gewichte können natürlicherweise eben so gut Multipla
derselben genommen werden, je nachdem es die Verdünnung der zu untersuchenden Säure
erfordert. Die Anzahl der Centigramme muß aber alsdann, damit sie dem Procentgehalte
entspreche, mit derselben Zahl dividirt werden, mit welcher man die Einheiten (die
sogleich zu bezeichnenden Zahlen) multiplicirt hat.
Diese Zahlen erhält man durch Division von 550 (2×275 [Aequivalent des
Kohlenstoffs]) in das Atomgewicht der betreffenden Säure, nach dem Ansaz:
Zwei Aequivalente Kohlensäure entsprechen einem Aequivalent der Säure, für welche die
Zahl zu finden ist, wie viel muß von lezterer genommen werden, damit die Kohlensäure
1,00 Gram. beträgt.
Um also z. B. die Zahl für Schwefelsäure zu finden, muß angesezt werden:
550 : 501
=
1,00 : x
x
=
0,91.
Um einen Anhaltspunkt zu geben, welches Multiplum der Einheitszahlen man etwa zur
Probe zu verwenden habe, schiken wir die Bemerkung voraus, daß es am zwekmäßigsten
ist, den Versuch so einzurichten, daß die entweichende Kohlensäure 1 bis 2 Gramme
beträgt.
1. Schwefelsäure.
Einheit des zu nehmenden Gewichts 0,91 Gram. (Man kann die
dritte Stelle, ohne das Resultat auf bemerkliche Weise zu verändern, weglassen.
Eigentlich müßte genommen werden 0,911 Gram.).
Multipla:
2
×
0,911
=
1,822
Gram.
3
×
—
=
2,733
—
4
×
—
=
3,644
—
5
×
—
=
4,555
—
6
×
—
=
5,466
—
7
×
—
=
6,377
—
8
×
—
=
7,288
—
9
×
—
=
8,199
—
10
×
—
=
9,110
—
15
×
—
=
13,650
—
Aus diesen Multiplen kann man ohne Rechnung alle irgend nöthigen finden, indem man,
im Falle eine Säure so schwach ist, daß das 15fache Multiplum die gehörige Menge
Kohlensäure noch nicht liefert, das 20,30,40fache u. s. w. anwendet — Zahlen,
die aus den 2,3,4fachen u. s. w. bloß durch Versezung des Komma's gefunden
werden.
Wenn man ins Auge faßt, daß das Quantum der wasserfreien Schwefelsäure dem Gewicht
der Kohlensäure, welche sie aus doppelt kohlensaurem Salz austreibt, nahe gleich ist
(0,91 geben 1,00), so ersieht man alsobald, welche Multipla für Schwefelsäure von
verschiedenen Verdünnungen die passendsten sind, damit das Quantum der Kohlensäure
in die oben angegebenen Gränzen (1 bis 2 Gramme Kohlensäure) hineinfalle.
Von gewöhnlicher englischer Schwefelsäure würde man also am zwekmäßigsten das
zweifache Multiplum, von officineller verdünnter (1 Schwefelsäure, 5 Wasser) etwa
das zehnfache anwenden.
2. Salpetersäure.
Einheit des zu nehmenden Gewichts 1,23 (genau 1,231).
Multipla:
2
×
1,231
=
2,46
Gram.
3
×
—
=
3,69
—
4
×
—
=
4,92
—
5
×
—
=
6,15
—
6
×
—
=
7,39
—
7
×
—
=
8,62
—
8
×
—
=
9,85
—
9
×
—
=
11,08
—
10
×
—
=
12,31
—
15
×
—
=
18,46
—
3. Salzsäure.
Einheit des zu nehmenden Gewichts 0,83 (genau 0,827).
Multipla:
2
×
0,827
=
1,654
Gram.
3
×
—
=
2,481
—
4
×
—
=
3,308
—
5
×
—
=
4,135
—
6
×
—
=
4,962
—
7
×
—
=
5,789
—
8
×
—
=
6,616
—
9
×
—
=
7,443
—
10
×
—
=
8,270
—
15
×
—
=
12,355
—
4. Citronensäure.
Einheit des zu nehmenden Gewichts 1,32 (genau 1,318).
Multipla:
2
×
1,318
=
2,636
Gram.
3
×
—
=
3,954
—
4
×
—
=
5,272
—
5
×
—
=
6,590
—
6
×
—
=
7,908
—
7
×
—
=
9,226
—
8
×
—
=
10,544
—
9
×
—
=
11,862
—
10
×
—
=
13,180
—
15
×
—
=
19,770
—
5. Weinsäure.
Einheit des zu nehmenden Gewichts 1,5 (genau 1,498).
Multipla:
2
×
1,498
=
2,996
Gram.
3
×
—
=
4,494
—
4
×
—
=
5,992
—
5
×
—
=
7,490
—
6
×
—
=
8,988
—
7
×
—
=
10,486
—
8
×
—
=
11,984
—
9
×
—
=
13,482
—
10
×
—
=
14,980
—
15
×
—
=
22,470
—
6. Essigsäure.
Einheit des zu nehmenden Gewichts 1,16 (genau 1,159).
Multipla:
2
×
1,159
=
2,318
Gram.
3
×
—
=
3,477
—
4
×
—
=
4,636
—
5
×
—
=
5,795
—
6
×
—
=
6,954
—
7
×
—
=
8,113
—
8
×
—
=
9,272
—
9
×
—
=
10,431
—
10
×
—
=
11,160
—
15
×
—
=
17,385
—
Da der Gehalt der im Handel vorkommenden Essige sich wenigstens einigermaßen gleich
bleibt, so läßt sich bei diesem eine bestimmtere Norm für die zu nehmende Menge
geben, als bei andern Säuren. Von starken Essigen nämlich wird das 60fache
Multiplum, von schwachen das 100fache eine genügende Menge Kohlensäure liefern.
II. Prüfung
des Braunsteins auf seinen Handelswerth.
Unter Braunstein versteht man im engsten Sinne des Wortes den Pyrolusit der Mineralogen, welcher in Gängen oder Nestern, meistens im
Porphyr begleitet von Barytspath, im Thonschiefer, auf Eisenerzgängen und Lagern
ziemlich verbreitet vorkommt und seiner chemischen Zusammensezung nach Mangansuperoxyd ist. Im weiteren gewöhnlicheren Sinne
begreift man darunter Gemenge von Pyrolusit mit den anderen natürlichen Oxyden des
Mangans, so wie den bleibrechenden Gangarten, wie solche auf den Gruben gewonnen und
in den Handel gebracht werden.
Bei der Anwendung des Braunsteins zur Chlorbereitung ist nur derjenige Sauerstoff wirksam,
welcher außer dem zur Bildung von Manganoxydul erforderlichen darin enthalten ist;
nur dieser sezt beim Zusammenkommen mit Salzsäure ein seinem Aequivalent
entsprechendes Quantum Chlor in Freiheit und man nennt ihn deßhalb den verwendbaren Sauerstoff des Braunsteins. Diesen
verwendbaren Sauerstoff will der Chlorfabrikant allein kaufen, die Menge desselben
bestimmt ihm den Werth des Braunsteins.
Außer diesem einen Punkt kommt jedoch auch noch ein zweiter in Betracht. Je nachdem
nämlich der reine Pyrolusit mit Mineralsubstanzen vermengt ist, welche, wie z. B.
der Schwerspath, von Salzsäure nicht angegriffen werben, oder mit solchen, welche
von lezterer aufgelöst werden, wie z. B. Eisenoxyd, Thonerde und Kalk, sind sehr
verschiedene Quantitäten Salzsäure erforderlich, um sein en verwendbaren
Sauerstoffgehalt zur Wirkung zu bringen. Der Werth des Braunsteins ist also auch
abhängig von der Quantität Säure, welche er zur Zersezung bedarf.
A) Prüfung des Braunsteins auf
seinen Gehalt an verwendbarem Sauerstoff. — Zu diesem Zwek schlugen
Berthier und Thomson vor,
die Kohlensäure zu bestimmen, welche der Braunstein durch Zersezung der Oxalsäure
(Kleesäure) entwikelt. Wenn ihre Methoden dem Zweke nicht völlig entsprachen, so lag
die Schuld nicht an dem Principe, sondern bloß an der Art der Ausführung. Unsere
Verfahrungsweise, durch welche alle Fehlerquellen möglichst vermieden werden, ist
folgende:
Man bringt eine gewogene Menge des fein zerriebenen Braunsteins in das Kölbchen A unseres alkalimetrischen Apparates (Fig. 85
Tab. III), fügt 2½ Theile oder etwas mehr
zerriebenen neutralen oxalsauren Kalis (durch Sättigen von gewöhnlichem Kleesalz mit
kohlensaurem Kali und Abdampfen zur Krystallisation leicht zu erhalten) oder 2
Theile neutralen oxalsauren Natrons und so viel Wasser hinzu, daß das Kölbchen
ungefähr zu ein Drittheil voll wird. Man dreht nunmehr den Stopfen auf A ein, tarirt den Apparat und saugt alsdann auf die S.
130 (im vorherg. Heft) beschriebene Art etwas Schwefelsäure aus B nach A herüber. Die
Entwikelung der Kohlensäure beginnt sogleich und zwar nicht stoßweise, sondern
äußerst gleichmäßig. Läßt sie nach, so saugt man wiederum etwas Schwefelsäure
herüber und fährt auf gleiche Weise fort, bis aller Braunstein zersezt ist, was
einen Zeitaufwand von 5 bis 10 Minuten erfordert, ohne jedoch fortwährende
Beaufsichtigung nothwendig zu machen. Die Zersezung erfolgt, wenn der Braunstein nur
irgend fein zerrieben war, überaus leicht und vollständig. Man erkennt ihre
Beendigung nicht nur an dem Aufhören der Kohlensäureentwikelung bei Gegenwart überschüssiger
Schwefelsäure, sondern auch daran, daß kein schwarzes
Pulver mehr am Boden des Kölbchens liegt. Zulezt saugt man etwas mehr Schwefelsäure
herüber, damit sich die im Kölbchen A enthaltene
Flüssigkeit stärker erhizt und die noch von derselben absorbirte Kohlensäure
vollständig ausgetrieben wird. Man lüpft alsdann das Wachsstöpfchen auf der Röhre
a, saugt Luft durch den Apparat, bis die lezte nicht
mehr nach Kohlensäure schmekt, läßt den Apparat erkalten und wägt ihn. Den ganzen
Versuch kann man sonach mit Leichtigkeit in einer Viertelstunde beendigen. Aus dem
Gewichtsverlust des Apparates (dem Gewicht der entwichenen Kohlensäure) findet man
die Quantität des im Braunstein enthaltenen verwendbaren Sauerstoffs oder, was
dasselbe sagen will, die Menge des darin vorhandenen Mangansuperoxyds durch
folgenden Ansaz:
Zwei Aequivalente Kohlensäure verhalten sich zu 1 Aeq. Mangansuperoxyd, wie die
gefundene Menge der Kohlensäure zu x; — x ist alsdann die in der angewendeten Menge Braunstein
enthalten gewesene Menge Superoxyd.
Gesezt wir hätten 4 Gramme Braunstein genommen und 3,5 Gr. Kohlensäure bekommen, so
müßten wir demzufolge ansezen:
550 : 546
=
3,50 : x
x
=
3,47.
In 4 Gram. Braunstein wären also 3,47 Gram. Superoxyd oder in 100 Theilen 86,7 Th.
enthalten gewesen.
Damit jedoch auch diese Rechnung unnöthig werde, darf man nur ausmitteln, welche
Menge Braunstein genommen werden müsse, damit die Anzahl der erhaltenen Centigramme
Kohlensäure die Procente an Mangansuperoxyd unmittelbar angibt. Man muß also
ansezen:
550 : 546
=
100 : x
x
=
0,993.
Nähme man demnach 0,993 Gram. Braunstein zu einem Versuche, so würden die Centigramme
der entwichenen Kohlensäure der unmittelbare Ausdruk für den Procentgehalt des
Braunsteins an Superoxyd seyn. Man würde aber alsdann eine zum genauen Wägen etwas
kleine Menge Kohlensäure erhalten. Es ist daher zwekmäßiger, ein Multiplum dieser
Einheitszahl zu nehmen und die Quantität der erhaltenen Centigramme Kohlensäure
alsdann durch die nämliche Zahl zu dividiren, mit welcher man die Einheit
multiplicirt hat. Als das geeignetste Multiplum erscheint uns das Dreifache oder
2,98 Gram.
Im Falle Braunsteinsorten kohlensaure alkalische Erden enthalten, wie dieß bei denen
gewisser Fundorte zuweilen der Fall ist, muß unserem Verfahren eine vorbereitende
Behandlung vorangehen. Braunsteine, die man in dieser Hinsicht noch nicht kennt, darf man nur
im gepulverten Zustande mit verdünnter Salpetersäure übergießen, um über die
Abwesenheit oder Gegenwart kohlensauren Kalks oder Baryts alsbald ins Reine zu
kommen. Findet Aufbrausen statt, so ist ihre Anwesenheit, findet keines statt, ihre
Abwesenheit erwiesen. Im ersteren Falle verfährt man alsdann auf folgende Art:
Man wägt, wie gewöhnlich, das vorgeschriebene Quantum Braunstein (2,98 Gram.) ab,
bringt es in das Kölbchen A, übergießt es darin mit sehr
verdünnter Salpetersäure (1 Salpetersäure, 20 Wasser) und läßt ein paar Minuten
stehen. Man gießt alsdann die überstehende Flüssigkeit auf ein kleines Papierfilter,
fügt zu dem im Kölbchen bleibenden Braunstein noch zwei- bis dreimal Wasser
und wäscht damit auch den auf dem Filtrum befindlichen, mit der Flüssigkeit
herausgespülten Braunstein nach. Man wirft nun das Filter sammt den darauf
befindlichen Braunsteintheilchen gerade wie es ist mit der Vorsicht in das Kölbchen,
daß von dem Braunstein nichts verloren geht und verfährt alsdann wie gewöhnlich.
B) Prüfung des Braunsteins mit
gleichzeitiger Berüksichtigung des Säurequantums, welches zu seiner
vollständigen Zersezung erfordert wird. — Es ist oben
auseinandergesezt worden, daß es in Bezug auf den Säureverbrauch bei der Bereitung
des Chlors nicht gleichgültig ist, von welcherlei Art die dem Mangansuperoxyd in den
gewöhnlichen Braunsteinsorten beigemengten Mineralien sind; wir haben darauf
aufmerksam gemacht, daß Thonerde, Eisen, Kalk, so wie niedrere Oxydationsstufen des
Mangans einen Mehrverbrauch an Säure erfordern, während Schwerspath und andere in
Säuren unlösliche Körper keinen derartigen Verlust veranlassen.
Sollte Jemand wünschen einen Braunstein auch in dieser Beziehung kennen zu lernen, so
wird er diesen Zwek neben dem der gewöhnlichen Braunsteinprüfung durch folgende
Modification unseres obigen Verfahrens mit vollkommener Sicherheit erreichen.
Man nimmt käufliche englische Schwefelsäure und bestimmt ihren Gehalt ein für allemal
nach der früher beschriebenen Weise oder auch mit einem genauen Aräometer. Daß sie
nach der Prüfung in einem gut verschlossenen Glase aufbewahrt werden müsse, wenn ihr
Gehalt sich nicht vermindern soll, versteht sich von selbst.
Von dieser Schwefelsäure wägt man so viel in das Kölbchen A. ab, daß die Quantität der in der abgewogenen Menge enthaltenen
wasserfreien Säure 5,47 Gram. beträgt. Die demnach zu nehmenden Gewichte ersieht man
aus der folgenden Tabelle:
Textabbildung Bd. 090, S. 223
Gefundenes specifisches Gewicht.;
Gefundener Procentgehalt an wasserfreier Saͤure.; Zu nehmendes
Gewicht.
In das Kölbchen bringt man ferner so viel Wasser, daß es zu ein Viertel voll wird und
endlich zwischen 6,5 und 7 Gram. neutralen oxalsauren Kalis oder zwischen 5,5 und 6
Gram. neutralen oxalsauren Natrons. Alsdann wägt man von dem zu prüfenden fein
zerriebenen Braunstein, der zuvor auf kohlensaure alkalische Erden geprüft worden
ist, 2,98 Gram. ab und bringt diese Menge in ein Glasröhrchen von derselben Größe
und Form, wie man sie bei der Acidimetrie gebraucht. In ein zweites derartiges
Röhrchen bringt man ungefähr eben so viel oder etwas mehr (auf genaue
Gewichtsbestimmung kommt es bei dieser Portion nicht an) gepulverten reinen
Pyrolusits.Zu diesem Zwek kann jeder Pyrolusit dienen, welcher frei ist von andern
Manganerzen. Enthaͤlt er Schwerspath, so ist er geradezu anwendbar,
enthaͤlt er Thonerde oder Kalk, so behandelt man ihn so lange in
gelinder Waͤrme mit verduͤnnter Salpetersaͤure, bis
alles Loͤsliche ausgezogen ist, waͤscht ihn alsdann mit Wasser
aus und troknet ihn. In Ermangelung von tauglichem Pyrolusit nimmt man
kuͤnstlich dargestelltes Mangansuperoxydhydrat. Man hängt
nun das mit dem zu prüfenden Braunstein gefüllte Röhrchen gerade so wie es S. 211
beschrieben ist, mittelst eines Fadens in das Kölbchen A
des zugerüsteten Apparates, stellt den Apparat auf die eine Waagschale und legt das
mit dem Pyrolusit gefüllte Röhrchen daneben. Auf die andere Waagschale bringt man
die Tara wie gewöhnlich.
Man lüpft alsdann den Kork auf A und läßt das Röhrchen
mit dem Braunstein in das Kölbchen fallen. Die Kohlensäureentwikelung beginnt
alsobald und dauert fort bis aller Braunstein zerlegt ist. Wenn dieselbe anfängt
langsamer zu werden, stellt man das Kölbchen A in
kochendes Wasser und läßt es darin bis keine Blasen mehr kommen. Sodann lüpft man
das WachskügelchenEs muß dieß nothwendig geschehen, waͤhrend das Koͤlbchen noch
in dem heißen Wasser steht, denn so wie man das leztere herausnimmt ohne die
Roͤhre a zu oͤffnen, steigt die
Schwefelsaͤure aus B zuruͤk und
der Versuch ist somit verdorben., nimmt A aus dem heißen Wasser und saugt die Kohlensäure aus. Der erkaltete und
abgetroknete Apparat wird wieder auf dieselbe Waagschale gebracht, auf welcher er
gestanden hatte und auf der das Röhrchen mit Pyrolusit noch liegt und die entwichene
Kohlensäure durch Gewichte substituirt. Die Anzahl der Centigramme, welche hiezu
nöthig sind, dividirt durch 3 gibt die Menge des im geprüften Braunstein enthaltenen
Superoxyds eben so wie oben in Procenten an.
Man nimmt jezt die aufgelegten Gewichte wieder weg, verändert aber im übrigen nichts
an der Tara und wirft nunmehr das Röhrchen mit Pyrolusit ebenfalls in das Kölbchen
A; das Wachskügelchen ist zuvor wieder aufgedrükt
worden. Beginnt keine neue Entwikelung von Kohlensäure mehr, so war der Braunstein
reiner Pyrolusit, so ist der Versuch beendigt. Beginnt aber eine neue Entwikelung,
so bringt man sie nach der eben angeführten Art, indem man A zulezt in heißes Wasser stellt, zu Ende. Nach dem Durchsaugen stellt man
den Apparat wiederum auf die Waage und legt auf dieselbe Schale 3 Gramme. Wird
dadurch das Gleichgewicht genau hergestellt, so hat kein Verlust an Säure
stattgefunden; der Braunstein enthält zwar Beimengungen, aber nur solche, welche
keine Säure in Anspruch nehmen. Sinkt aber die Schale mit dem Apparat, so ist es
sicher, daß ein Theil der Säure zur Bindung beigemengter Oxyde gedient hat. Die
Anzahl der Centigramme, welche an den 3 Grammen fehlen, welche also zu der Tara gelegt werden müssen, um das Gleichgewicht
herzustellen, multiplicirt mit 0,6114 gibt unmittelbar an, wie viel wasserfreie
Schwefelsäure bei Zersezung von 100 Theilen des geprüften Braunsteins ohne Nuzen für
die Chlorbereitung verbraucht wird. Dieselbe Zahl multiplicirt mit 0,333 besagt, wie
viel man zur Zersezung des Braunsteins Schwefelsäure ohne Nuzen verbraucht, so oft
man 100 Theile der lezteren verwendet. — Dieselbe Zahl multiplicirt mit
0,5552 zeigt an, wie viel wasserfreie Salzsäure man bei Zersezung von 100 Theilen
Braunstein unnüz verwendet. Dieselbe Zahl multiplicirt mit 0,333 gibt an, wie viel Salzsäure
vergeudet wird, so oft man 100 Theile derselben verbraucht.
Princip der beschriebenen Verfahrungsweisen. — Die
Grundlage unserer Methoden wird aus dem Folgenden leicht verständlich werden.
1 Aeq. Mangansuperoxyd können wir uns zusammengesezt denken aus
1 Aeq. Manganoxydul und aus
1 Aeq. Sauerstoff.
Will man den Sauerstoff als Chlor erhalten, so werden dazu 2 Aeq. Salzsäure
erfordert. Eines verbindet sich mit dem Manganoxydul zu salzsaurem Manganoxydul
(Manganchlorür und Wasser), aus dem andern wird alles Chlor in Freiheit gesezt,
indem sich sein Wasserstoff mit dem Aeq. Sauerstoff zu Wasser vereinigt. Ersezt man
die Salzsäure durch Schwefelsäure und Kochsalz, so braucht man 2 Aeq. Schwefelsäure.
Will man den Sauerstoffüberschuß des Superoxyds als Kohlensäure erhalten, so sind 2
Aeq. Oxalsäure nöthig; ersezt man die Oxalsäure durch Schwefelsäure und oxalsaures
Kali, so werden ebenfalls 2 Aeq. Schwefelsäure erfordert.
Nach dem angegebenen Verfahren sollen 2,98 Gram. Braunstein zusammengebracht werben
mit so viel Schwefelsäure, daß darin 5,47 Gram. wasserfreie Schwefelsäure enthalten
ist. Diese Zahlen stehen in dem Verhältniß wie 1 Aeq. Mangansuperoxyd zu 2 Aeq.
Schwefelsäure. Ist der Braunstein reines Superoxyd, so bleibt demnach bei Gegenwart
von überschüssigem oxalsaurem Kali nach geschehener Einwirkung weder Mangansuperoxyd
noch Schwefelsäure übrig. Die Schwefelsäure hat zur Hälfte schwefelsaures
Manganoxydul, zur andern Hälfte schwefelsaures Kali gebildet. Die frei gewordene
Oxalsäure ist durch Aufnahme des entbundenen Sauerstoffs in 2 Aeq. Kohlensäure
übergeführt worden. Bringt man eine weitere Menge Braunstein hinzu, so erhält man
keine Kohlensäure mehr, es ist ja keine Schwefelsäure mehr da, um Oxalsäure in
Freiheit zu sezen.
Daß man aus der Quantität der erhaltenen Kohlensäure die Menge des verwendbaren
Sauerstoffs (des Mangansuperoxyds) ersehen könne, braucht hier nicht mehr erwähnt zu
werden, indem diese Sache schon oben auseinander gesezt worden ist. Daß man aber aus
der Menge der erhaltenen Kohlensäure auch die Menge der zur Zersezung des
Mangansuperoxyds verwendeten Schwefelsäure finden kann, erscheint eben so klar,
wenn man sich erinnert, daß man für je ein Aeq. derjenigen Schwefelsäure, welche
dazu gedient hat Oxalsäure in Freiheit zu sezen, oder welche, wenn wir uns an der
Stelle des kleesauren Kalis Kochsalz denken, dazu gedient haben würde, Salzsäure und
somit Chlor abzuscheiden, 2 Aeq. Kohlensäure erhält, oder, was das Nämliche ist, für
je ein Aeq. der überhaupt zur Zersezung des
Mangansuperoxyds verbrauchten Schwefelsäure, ein Aeq. Kohlensäure.
Betrachten wir nun die Veränderungen, welche eintreten werden, wenn der Braunstein
kein reines Superoxyd ist, sondern außer diesem noch Manganoxydhydrat, oder Eisen,
oder Kalk, oder Schwerspath enthält.
Den Gehalt des Braunsteins an Superoxyd werden wir unter allen Umständen richtig
finden. Schwefelsäure ist ja im Ueberschuß, kleesaures Kali in genügender Menge
vorhanden, kurz alle Bedingungen sind ja erfüllt, die wir eben als nothwendig
erkannt haben.
Um uns nun das Verhältniß des Säureverbrauchs klar zu machen, wollen wir uns erst den
Braunstein als aus 3 Aeq. Mangansuperoxyd und 2 Aeq. Schwerspath gemengt denken.
Wir bringen ihn bei Gegenwart von oxalsaurem Kali zusammen mit 10 Aeq. Schwefelsäure.
Wäre der genommene Braunstein reines Superoxyd, so würden wir erhalten 10 Aeq.
Kohlensäure, das ist für 5,47 Gram. (die zu nehmende Menge) Schwefelsäure 3,00 Gr.
Kohlensäure, denn
501 : 275 = 5,47 : 3,00.
Im gesezten Falle erhalten wir aber nur 6 Aeq. Kohlensäure, die 4 Aeq. außerdem durch
die Schwefelsäure noch in Freiheit gesezter Oxalsäure bleiben als solche in Lösung,
indem kein Sauerstoff mehr da ist, der sie in Kohlensäure verwandeln könnte. Bringen
wir neues Mangansuperoxyd hinzu, so bekommen wir von diesen 4 Aeq. Oxalsäure noch 2
als Kohlensäure, und zwar erhalten wir dafür 4 Aeq. von lezterer. — Wir
erhielten zuerst 6 Aeq., wir erhielten ferner 4 Aeq., zusammen also 10 Aeq.
Kohlensäure, d. i. die Quantität, welche aus der genommenen Schwefelsäure entwikelt
werden mußte, wenn keine anderweitig in Anspruch genommen worden ist.
Sezen wir jezt statt des Schwerspaths, um den Fall recht einfach zu machen,
Manganoxydul oder Kalk, so erhalten wir zuerst ebenfalls nur 6 Aeq. Kohlensäure, in
der Flüssigkeit bleiben 4 Aeq. Schwefelsäure oder richtiger Oxalsäure, welche mit
Mangansuperoxyd noch nicht in Gegenwirkung gekommen sind. Von diesen 4 Aeq.
sind jedoch zwei nicht frei, sondern in Verbindung mit dem Manganoxydul oder
Kalk vorhanden. Sezen wir daher jezt mehr Mangansuperoxyd hinzu, so bekommen wir
diesem Umstand zufolge nicht 4 Aeq., sondern nur 2 Aeq. Kohlensäure. Wir
erhalten demnach im Ganzen 8 Aeq., wir hätten erhalten müssen 10 Aeq. Die den
fehlenden 2 Aeq. Kohlensäure entsprechenden 2 Aeq. Schwefelsäure sind demnach
für die Kohlensäurebildung oder, wenn wir statt des oxalsauren Kalis Kochsalz
sezen, für die Chlorbereitung verloren gegangen.
Drükt man die Sache allgemein aus, so muß demnach gesagt werden:
Die Menge der Kohlensäure, welche man bei dem Verfahren weniger
erhält als der angewandten Schwefelsäure entspricht, ist nach einfachen
Aequivalenten proportional dem Verlust, den man an lezterer durch andere
Substanzen erlitten hat.
Im Falle ein Braunstein kohlensauren Kalk enthalten
sollte, so muß (wie bei der vorhergehenden Prüfungsmethode) zuvor mit einem Theile
desselben die Kohlensäure nach unserer alkalimetrischen Methode bestimmt werden, ehe
man die Resultate berechnen kann. Die aus 2,98 Gram. des Braunsteins erhaltene Menge
wird alsdann sowohl von der ersten als von der zweiten Gewichtsabnahme abgezogen,
alles Uebrige aber bleibt sich gleich. Daß man bei einem geringen Gehalte von
kohlensaurem Kalk zwekmäßiger ein Multiplum der Zahl 2,98 von dem Braunstein nimmt
und die erhaltene Kohlensäure alsdann auf diese Menge berechnet, liegt auf der
Hand.Die Verfasser theilen in ihrem Werke zwei Tabellen
mit, um sowohl die Menge der zur Chlorgewinnung wirklich in Anwendung
kommenden Salzsäure, als die Quantitaͤt der unnuͤz zu
verwendenden Saͤure, fuͤr jeden auf obige Weise
gepruͤften Braunstein schnell bestimmen zu koͤnnen.A. d. R.
Tafeln